极端高温下植物如何幸存?景天酸(CAM)光合作用助力二叠纪—三叠纪大灭绝后的植物复苏
2024年4月20日,中国地质大学(武汉)喻建新教授团队和英国利兹大学徐珍博士后联合多国科研单位,在 Nature Ecology & Evolution 发表题为 CAM photosynthesis may have conferred an advantage during the Permian–Triassic mass extinction event 的研究论文(原文链接:https://doi.org/10.1038/s41559-026-03026-0)。

如果把二叠纪末大灭绝后的陆地生态恢复看作一场极端环境下的“生存筛选”,这项研究提供了一条具有解释力的关键线索:在超级温室气候、强热胁迫和生态系统重组的背景下,早三叠世迅速扩张的草本石松类(如脊囊等),并非只是“偶然幸存”,而很可能具备一种关键生理优势——景天酸光合作用(CAM)。
本研究将形态学系统发育分析、植物有机碳同位素证据与气候模拟整合在统一框架下,提出早三叠世优势草本石松类,很可能类似于其现生近缘类群水韭属(Isoetes),具备更强的耐高温和环境胁迫适应能力。这一工作为理解地球最大生物灭绝事件后的陆地植被响应与生态系统重建机制提供了关键证据。

图1. 本论文研究对象:华南三叠纪石松繁殖器官孢子穗,总长度约6厘米。徐珍、冉维菊、郭宴华于2019年末采集于湖南省。
研究背景
二叠纪—三叠纪大灭绝(约2.52亿年前)是地球历史上最严重的一次生物危机。由西伯利亚暗色岩大规模火山活动引发,全球气温快速上升约6–10℃,大气CO₂浓度升至现代的4倍以上。海洋生物灭绝率超过90%,陆地脊椎动物科级损失超过70%。
陆地植被也经历剧烈更替。古生代优势的高大植物(如鳞木、大羽羊齿、科达等)迅速消亡,而低矮草本石松类在早三叠世广泛占据低地生态位,成为灾后最重要的“灾难分子”。然而,它们为何能够在极端高温和高CO₂环境中存活并迅速扩张,长期缺乏明确的生理机制解释。
由于植物化石记录的是某一时刻的形态,而生理过程是连续动态的,难以直接保存在岩石中,因此本研究从三个方面重建其生理机制:
1.系统发育关系:确定这些灾难植物与现生植物的亲缘关系,从最近缘类群推测生理特征;
2.地球化学证据:利用植物碳同位素信号反映不同光合作用类型;
3.气候约束:在地球系统模型重建的极端高温背景下,检验该生理策略的合理性。
数据与方法
研究团队对中国华南及全球晚二叠世至中三叠世的485件石松类孢子叶化石开展形态学定量拓扑研究,基于127个形态性状进行主成分分析(PCA)与邻域网络分析(NNA),以重建二叠纪—三叠纪过渡期优势石松类的形态关系与系统发育位置。结果显示,三叠纪优势类群脊囊(Tomiostrobus,同物异名 Annalepis)与现代水韭属(Isoetes)具有最近的系统发育关系。二者在孢子叶形态、生长习性和繁殖结构等关键性状上高度保守。由于植物形态往往服务于功能,这种高度形态相似性表明,灭绝后优势石松类很可能属于水韭目,并具备类似现代水韭类群的生理可塑性基础。
方法上,文章并非简单判断化石“长得像不像”,而是基于127个形态性状构建数据库,首先利用主成分分析(PCA)定量刻画各石松类植物在形态空间中的分布,并清理形态空间高度重叠的同物异名属种,从而实现石松类化石鉴定的数字化。由于植物普遍存在异叶性,同一植株上不同生长位置、不同发育年龄的器官形态通常存在差异,因此PCA分析中各属种表现为一个形态空间,而不是重叠于单一坐标点,这也反映了异叶性对化石鉴定的影响。基于此,本研究选取距离各形态空间质心最近的标本,作为最能代表该属种形态特征的“模式种”。需要说明的是,这里的“模式种”仅用于本研究的定量分析,并不完全等同于各形态种建种时的分类学模式种。用其代替整个属种内所有标本进行系统发育分析,从理论上更接近分类学意义上的生物种,而非仅由保存形态定义的化石(器官)形态种。
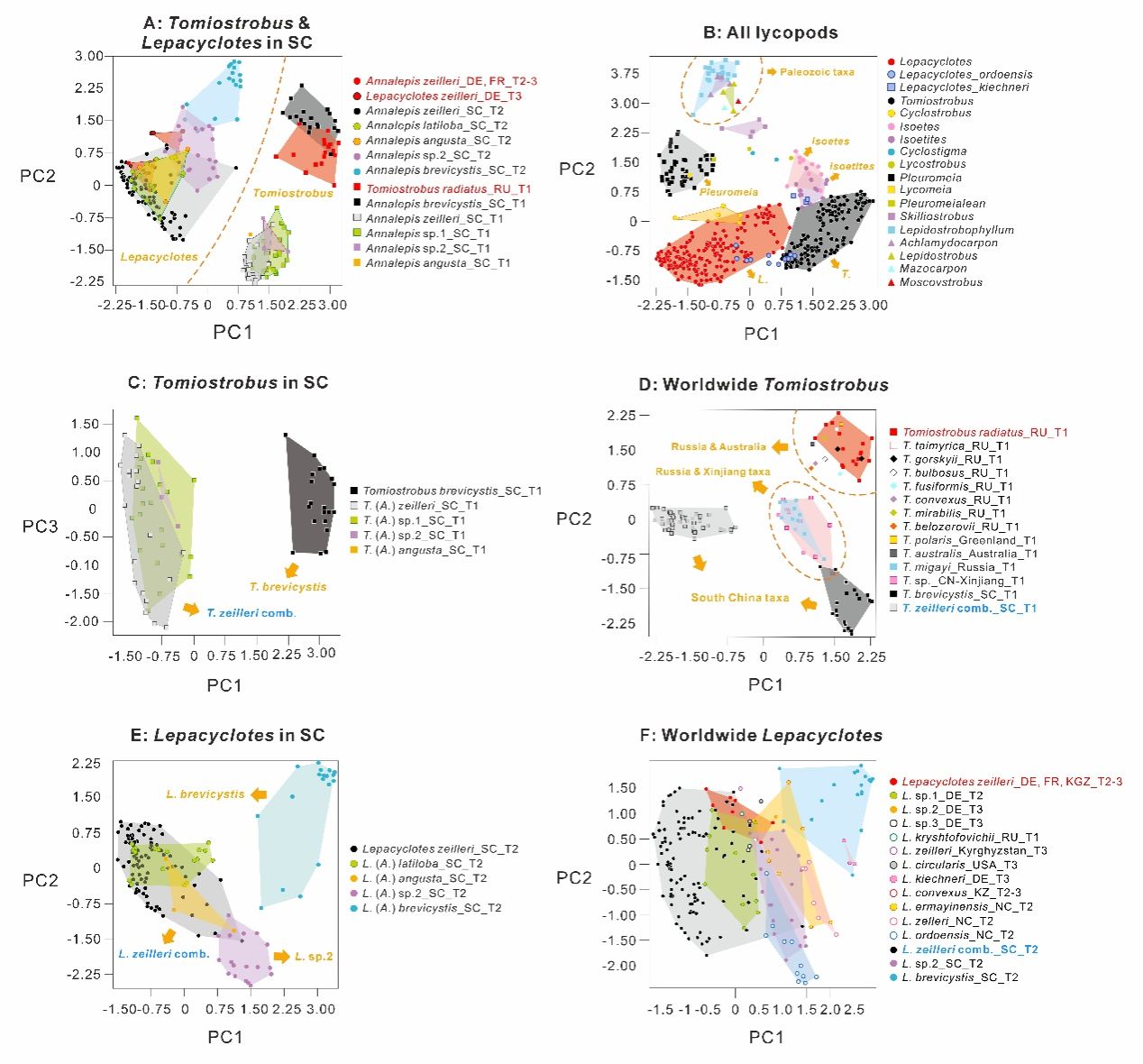
图2. 石松类孢子叶形态二维主成分分析(PCA)结果:a为华南地区Tomiostrobus与Lepacyclotes孢子叶分析;b为显生宙代表性石松类孢子叶分析;c为华南地区Tomiostrobus孢子叶分析;d为全球Tomiostrobus 孢子叶分析;e为华南地区Lepacyclotes孢子叶分析;f为全球Lepacyclotes 孢子叶分析,展示不同类群形态空间分布与分类聚类特征。
在通过PCA形态空间质心确定代表性“模式种”后,本研究进一步采用邻域网络分析NEE,对这些模式种的形态性状数据库进行系统发育分析。不同于传统系统发育树常用的最大简约法,邻域网络分析NEE能够将全部形态性状纳入分析,并以网络形式呈现那些不直接参与树状分枝、但仍然携带演化或功能信息的性状。对于古生物研究而言,许多形态特征在功能或演化上的权重并不明确,因此邻域网络分析具有独特优势,可以减少人为筛选形态性状对系统发育结果造成的影响。
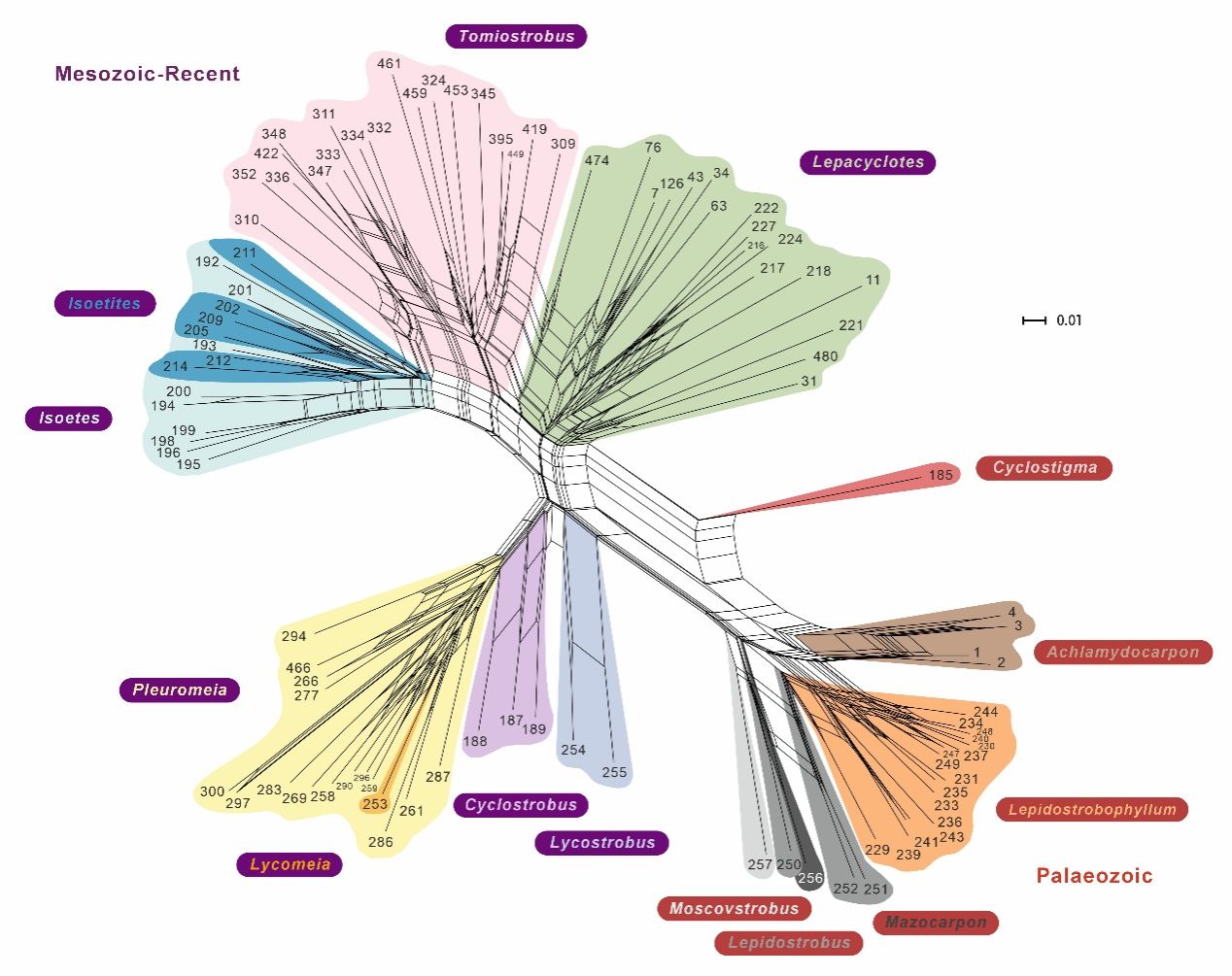
图3. 所有石松类物种孢子叶邻域网络图:展示各化石类群与现代水韭的形态距离与系统发育关系,标注分支对应物种编号。
在确定三叠纪石松脊囊与现代水韭具有最近亲缘关系后,研究进一步系统梳理了现生水韭的生理特征。现代水韭具有特殊的兼性CAM光合作用能力,在受到高温、干旱或水生环境中CO₂供应不足等胁迫时,可以从C3光合作用灵活切换至CAM景天酸光合作用。基于这种亲缘关系和生理类比,本研究进一步提出,水韭的古代近缘类群,即三叠纪草本石松脊囊,也可能具有类似的兼性CAM光合作用能力。
不同光合作用途径产生的光合产物具有不同的碳同位素特征。现代植物中主要存在三种光合作用途径,即C3、C4和CAM,但C4光合作用主要存在于被子植物中,在二叠纪—三叠纪时期尚未出现。C3植物主要通过Rubisco蛋白固定CO₂,而Rubisco对轻碳同位素¹⟡C具有更强的分馏偏好;同时,C3植物在白天光合作用时开放气孔,叶片内部CO₂与大气持续交换,因此植物体碳同位素值通常相对偏轻,即表现为负偏。相比之下,CAM植物为避开白天高温和干旱胁迫,通常在夜间打开气孔,通过PEP羧化酶固定CO₂,并将其转化为苹果酸储存在液泡中;白天则关闭气孔,以减少水分散失和光呼吸,并利用夜间储存的CO₂进行光合作用。由于PEP羧化酶对碳同位素的分馏效应较弱,且白天气孔关闭后光合作用系统相对封闭,CAM植物的碳同位素值通常相对偏重,即表现为正偏。兼性CAM植物可在C3与CAM之间切换,因此植物体碳同位素特征取决于C3与CAM固碳贡献的相对比例,而这一比例又受到干旱、高温等环境胁迫强度控制。
由于碳同位素不仅受光合作用途径影响,也会受到环境因素和大气CO₂浓度变化控制,因此在样品选择上,本研究仅选取华南地区产自相似沉积环境的植物标本,并仅在各时代内部比较石松类与非石松类植物的碳同位素差异。考虑到陆相地层定年的困难,本研究在测量植物体碳同位素的同时,也测量了同层围岩的碳同位素。一方面,这可以帮助确认测量对象为植物实体碳,而非后期形成的印模或围岩有机质;另一方面,也可用于判断不同剖面样品是否处于相近层位。该方法尤其适用于二叠纪—三叠纪之交的研究,因为大灭绝期间快速而剧烈的碳同位素波动在区域上具有较好一致性。结果显示,二叠纪—三叠纪之交石松类植物的碳同位素值比同期非石松类植物偏重约3.35‰。这一差异在灭绝前并不存在,并随着中三叠世气温降低而明显减小,表明三叠纪草本石松类很可能采用了兼性CAM光合作用,并可能部分利用沉积物或水体中的CO₂。
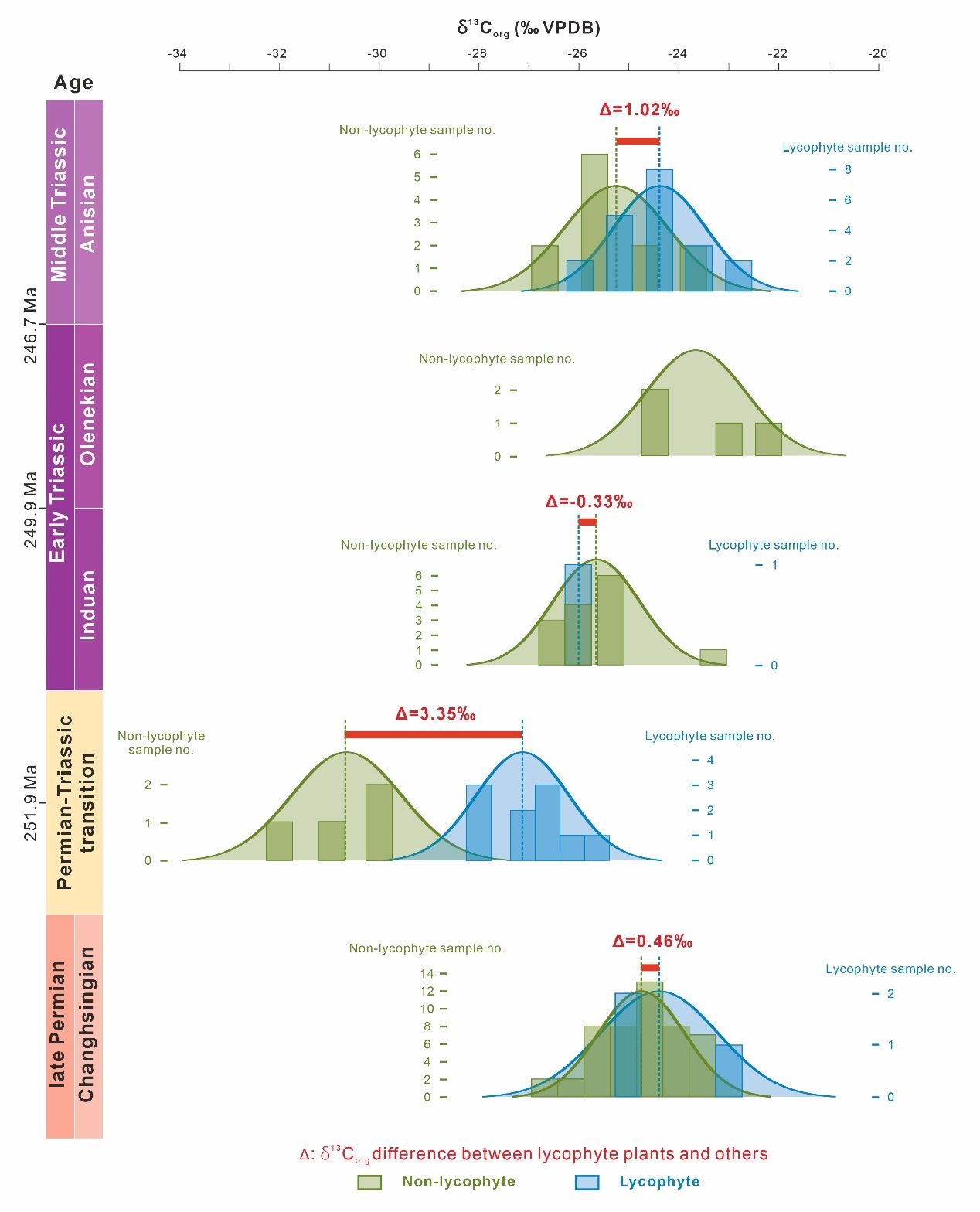
图4. 华南地区晚二叠世至中三叠世植物化石有机碳同位素值及石松类与其他植物碳同位素差值:展示不同时期石松类与非石松类植物δ¹³Corg差异,反映光合途径差异。
第三条证据来自气候模拟。研究调用HadCM3BL地球系统模型,重建了晚二叠世、灭绝过渡期和早三叠世三个关键时段的平均与极端日最高地表温度,并将石松类宏体化石和孢粉化石出现地点叠加到古地理温度场上,以评估这些植物当时实际面临的热环境。结果表明,草本石松类可以在超过40℃的地区生存,部分地区温度甚至超过65℃。在这样的高温条件下,典型C3植物的光合作用会受到严重限制,包括Rubisco activase失活、光呼吸急剧增强、气孔关闭以及光合电子传递受阻等,导致其难以维持稳定的碳同化能力。同时,C4光合作用在该时期尚未起源,因此CAM光合作用可能是这一极端温室气候下最具解释力的优势光合策略之一。
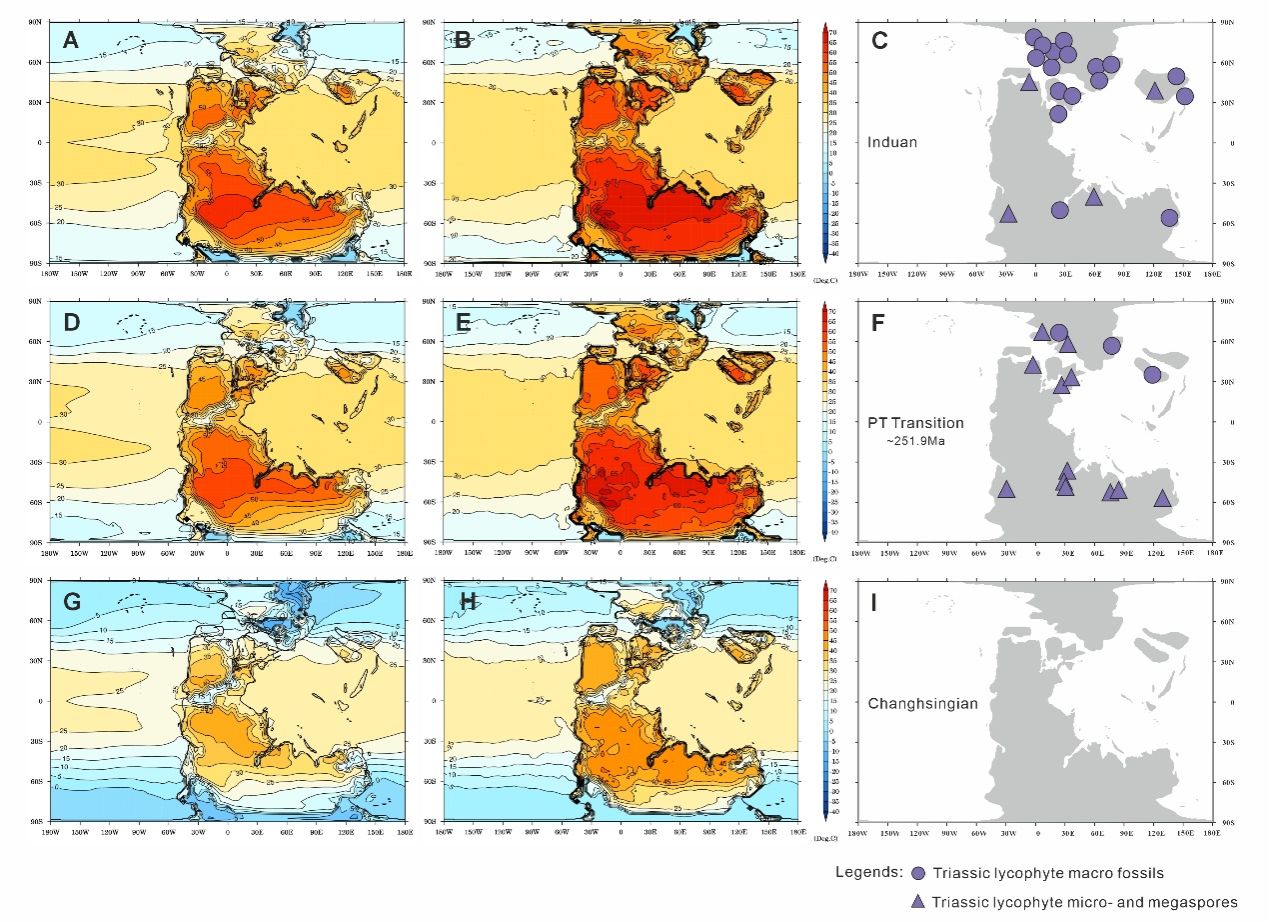
图5. 三叠世石松类大化石和孢子化石分布及HadCM3BL模拟的地表温度:a–b、d–e、g–h分别为印度期、过渡期、长兴期平均与极端日均地表温度;c、f、i为对应时期石松类化石分布,显示其在极端高温区的广泛分布。
结论
综合形态学、碳同位素与气候模拟等多方面证据,研究表明,CAM光合代谢为石松类在极端温室气候下存活提供了一种简洁且具有解释力的机制。现代水韭作为其现存后裔,保留了兼性CAM光合作用、根系吸收沉积物CO₂以及高温休眠等关键生存策略。二叠纪—三叠纪过渡期CAM型草本石松的广泛分布,表明这一类群不仅成功适应了极端环境,也维持了最基本的陆地植被覆盖,从而避免生态系统发生完全崩溃。
然而,需要指出的是,CAM光合作用的碳同化效率通常低于C3植物。因此,如果在大尺度上发生由C3向CAM的光合作用模式转换,可能导致陆地生态系统整体生产力下降,并减少有机碳埋藏,进而通过生物地球化学反馈对气候系统产生影响,甚至在一定程度上放大变暖趋势。
从演化角度来看,二叠纪—三叠纪之交的草本石松类可能代表了目前已知最早的CAM光合作用记录。在后续演化过程中,该光合作用模式在侏罗纪裸子植物(如苏铁类)以及多个被子植物类群中多次出现。CAM在不同植物类群中的独立演化,表明其相关生理与遗传机制可能具有较为古老的起源,也暗示现代多数植物可能在一定程度上具备启动CAM光合作用的潜在能力。
自二叠纪—三叠纪之后,地球经历了多次显著的气候变暖事件,包括当前的人为全球变暖过程。在这些背景下,植物在历史上形成的生理适应机制,可能在未来持续升温过程中再次发挥作用。因此,深入研究这些生理过程及其在不同环境条件下的转换,将有助于理解陆地生态系统对气候变化的响应方式。这也是本研究关注已灭绝植物生理过程的核心原因——其本质在于探索植物长期演化过程中形成的“生理基因库”。即使相关类群已经灭绝,这些古老的生理潜力仍可能在相似环境胁迫下以不同形式再次出现,从而为预测未来陆地植被对升温的响应提供关键参照。
总体而言,该研究首次将化石形态学证据、同位素生理信息与地球系统气候模拟相结合,系统揭示了CAM光合代谢在深时重大环境危机中的潜在适应价值。不仅完善了二叠纪—三叠纪陆地植被更替的机制链条,也为理解未来全球变暖背景下陆地生物圈的演化趋势提供了重要的古生物学视角。
限制与边界
这篇文章值得肯定的是证据链比较完整,但边界也要说清楚。
第一,CAM 在现生植物中的严格判据通常依赖夜间苹果酸积累等生理过程,而化石材料显然无法直接测试。因此,论文给出的不是“直接观察到的 CAM”,而是基于形态近缘性、碳同位素特征和古气候约束做出的综合推断。
第二,碳同位素信号本身会受到大气 CO2 组成、沉积物有机质分解、水体无机碳来源等多重因素影响,因此作者也明确承认,现有数据还不足以定量计算这些石松类到底有多大比例依赖 CAM。
第三,这项研究重点解释的是二叠纪末到早三叠世先锋石松类为何能在极端环境中扩张,它并不意味着当时所有植物恢复过程都由同一种机制控制。更广泛的陆地生态恢复,仍然需要结合不同植物类群、不同沉积环境和更高时间分辨率的记录继续检验。
展望
如果这条解释链继续被更多化石、生理类比和模型结果支持,它的重要意义会超出古植物学本身。因为它提示我们,极端气候事件后的生态恢复,不仅取决于“谁先占据空位”,还取决于哪些生理策略真正能在高温、高 CO2、强水分胁迫下维持碳吸收与生存。换句话说,二叠纪末植物恢复史,可能也是一次深时尺度上的“极端气候生理筛选实验”。
本研究自2014年开始,受到各位老师同学的大力帮助,以及国家自然科学基金项目的经费支持,以下为致谢名单,再次感谢:
We thank H. F. Yin, F. S. Meng, W. J. Ran, Q. Xue, Y. H. Guo, X. Shi, W. C. Shu, L. Zhang, Y. Y. Tian, X. J. Wang, M. J. Zhang, G. Z. Xu, B. B. Li, M. Fan and W. J. Lin for fieldwork assistance and H. F. Yin, J. Y. Wan, A. H. Yuan, S. Z. Gu and M. H. Zhang for help with clustering methods and for discussion of results. A. Spencer is thanked for help with neighbourhood network methods and E. Kustatscher, D. Royer and R. Bateman for thoughtful discussion on all aspects of this work. We thank Q. P. He for making the reference searching program. G. M. Luo, X. Y. Ma, B. Chang, K. P. Ewert, X. Q. Zhang, D. D. Li, H. Zhao, L. S. Zhao, L. Zhang, Y. Du and H. Y. Song are also thanked for assistance with carbon isotopes experiments. This work is financially supported by the National Natural Science Foundation of China (grant 42430209) (J.Y., Z.X., N.P.), UK Research and Innovation project EP/Y008790/1 (Z.X., B.J.W.M.), Natural Environment Research Council NE/T000392/1 (B.H.L.), Human Frontiers Science Program grant RGP0066/2021 (B.H.L.), the UK Palaeontological Association Sylvester-Bradley Award PA-SB202406 (Z.X.) and the US National Science Foundation (FRES 2121594) (I.P.M., Z.X.). We thank Y. Chi for colouring the reconstructions in the figures. We thank Zheng Dongyu and Wang Yuxuan for helping to produce this press release.

图6. 团队野外工作照片